- Cellule CAR-T: La Terapia con Linfociti T che Portano Recettori Chimerici.
- Cosa Sono le Cellule CAR-T
- Un Segmento di DNA Artificiale è introdotto nei Linfociti dei Pazienti
- Rischi Connessi con la Terapia CAR-T
- Le Cellule CAR-T sono una Terapia Viva
- Le Cellule CAR-T sono una Terapia Prototipo
- Problematiche Logistiche e Aspetti Pratici
- Indicazioni Previste (Ottobre 2025)
Cellule CAR-T: La Terapia con Linfociti T che Portano Recettori Chimerici.
Le cellule CAR-T sono una nuova terapia, approvata dagli organi regolamentatori FDA e EMA tra il 2017 e il 2018. Questa terapia è indicata in alcune neoplasie ematologiche come i linfomi a cellule B e il mieloma multiplo.
Si tratta di una terapia cellulare, cioè una terapia la cui azione antineoplastica è svolta da cellule viventi che sono di origine autologa (ottenute dallo stesso paziente). Queste cellule sono linfociti di tipo T ed assumono capacità antineoplastica dopo modifiche genetiche ed espansione in vitro.
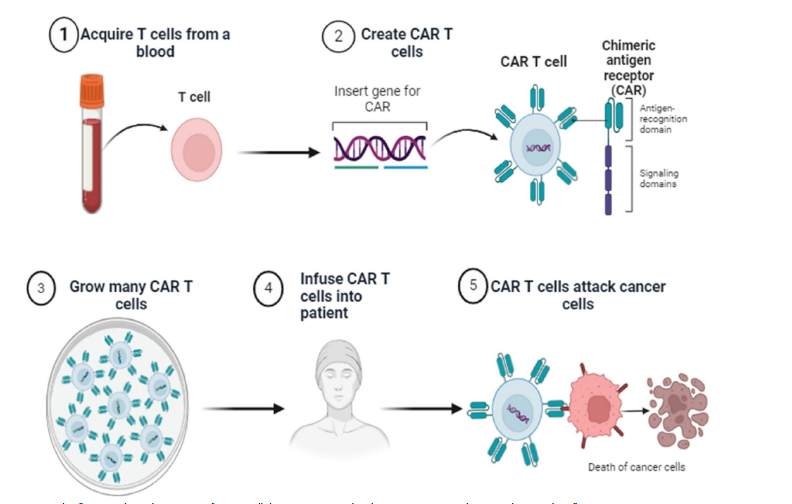
Al momento, le cellule CAR-T di origine autologa sono state approvate dalla FDA e dall’EMA per il trattamento dei linfomi a cellule B in ricaduta o primitivamente refrattari e per il mieloma multiplo refrattario ad almeno 3 agenti differenti (daratumumab, inibitore del proteasoma e immunomodulante).
Se queste sono le indicazioni recepite dagli organi regolatori, però studi clinici prospettici e controllati sono in corso per studiare i risultati di un loro impiego più precoce in fasi di malattia meno avanzate in pazienti non ancora divenuti refrattari.
L’efficacia delle cellule CAR-T è stata dimostrata ed approvata anche in pazienti affetti da leucemia linfoblastica acuta che interessa i linfociti B.
Cosa Sono le Cellule CAR-T
Le cellule CAR-T sono linfociti T che hanno subito una modifica dei loro geni; in tal senso è una terapia genica.

Questa modificazione genica consiste nell’introduzione nel nucleo della cellula di un segmento di DNA costruito in laboratorio che la rende capace di riconoscere i linfociti B e di lisarli.
La modifica genetica viene ottenuta con l’ausilio di un virus appartenente alla classe dei lentivirus. Il virus viene reso “difettivo” nel senso che è in grado di penetrare in vitro nei linfociti che si vogliono modificare e di introdurre nel DNA dei linfociti il gene prescelto, anch’esso costruito in vitro. Questi virus difettivi sono incapaci di replicarsi e, una volta svolto il loro compito, hanno breve vita.
Un Segmento di DNA Artificiale è introdotto nei Linfociti dei Pazienti
Le terapie con cellule CAR-T fin qui approvate dalla FDA e dall’EMA hanno effetto antineoplastico. Il DNA introdotto nelle cellule codifica per una struttura recettoriale creata con tecniche di ingegneria genetica e che non è presente in natura. Il trascritto di questo gene si localizza sulla superficie del linfocita (RECETTORE DI SUPERFICE) e lo “arma”, rendendolo in grado di riconoscere l’antigene CD19 o l’antigene BCMA presenti sulle cellule neoplastiche di linfoma o di mieloma e di ucciderle.
Questa struttura che si localizza sulla superficie cellulare è stata denominata RECETTORE CHIMERICO PER L’ANTIGENE (CHYMERIC ANTIGEN RECEPTOR) e nel caso del paziente affetto da linfoma o da leucemia acuta linfoblastica è in grado di riconoscere e uccidere le cellule linfomatose che portano sulla loro superficie l’antigene CD19.
Mentre nel caso di pazienti affetti da mieloma multiplo i linfociti del paziente sono preliminarmente raccolti e viene introdotto un gene che codifica per un recettore di membrana in grado di riconoscere sulle plasmacellule neoplastiche l’antigene BCMA (B cell maturation antigen).
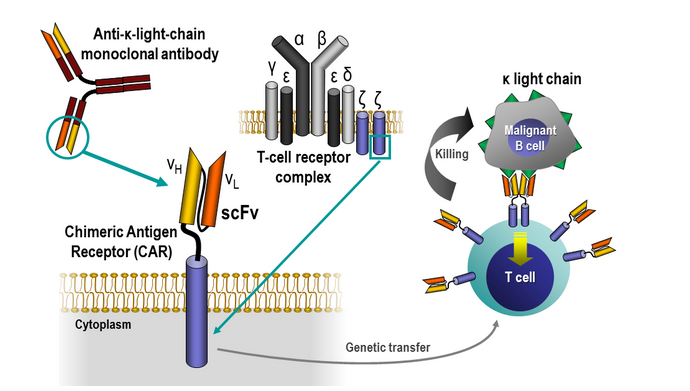
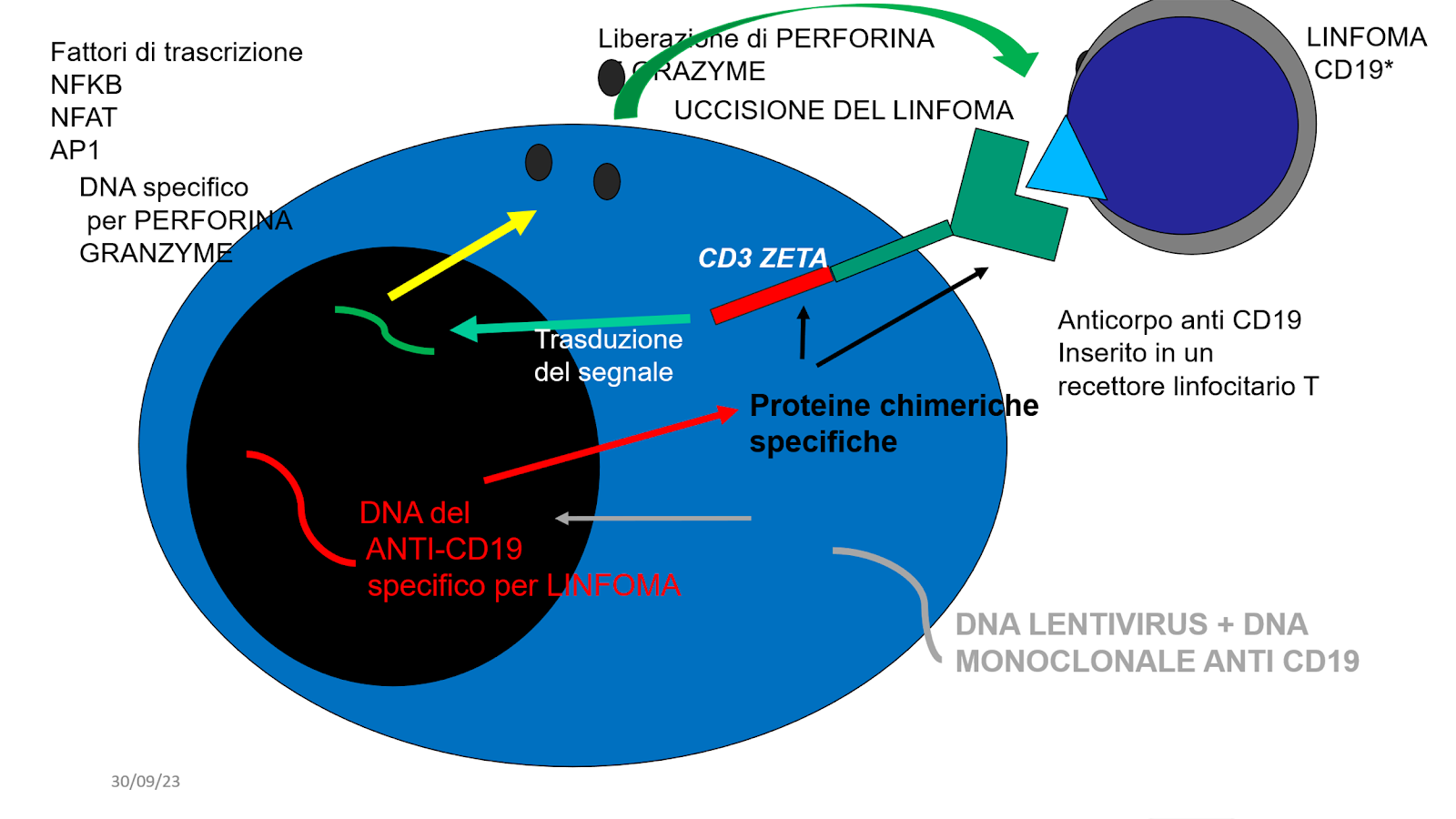
Questo segmento di DNA comprende una porzione che riconosce l’antigene CD19 e una porzione, denominata CD3 zeta, capace di ricevere il messaggio di riconoscimento dell’antigene da parte del recettore e di innescare la cascata di eventi citoplasmatici e nucleari che attiva il linfocita e lo rende in grado di lisare le cellule neoplastiche che ad esso si sono legate.
Ulteriori miglioramenti sono stati ottenuti con la creazione di un recettore chimerico comprendente una struttura coattivatoria (CD28 o 41bb)
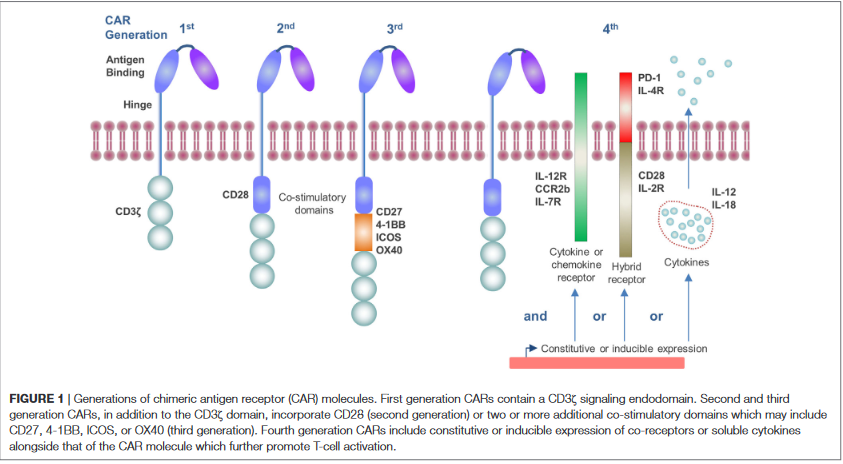
Rischi Connessi con la Terapia CAR-T
La terapia con cellule CAR-T comporta, come tutte le terapie mediche, dei rischi che in questo caso non sono irrilevanti.
Circa un terzo dei pazienti presenta una sindrome denominata sindrome da liberazione da citochine (CRS) che è caratterizzata da febbre, ipotensione e ipossiemia. Tale sindrome, alquanto precoce dopo l’infusione di cellule CAR-T, può necessitare di terapia intensiva, con idratazione, agenti vasopressori ed ossigenoterapia. La sua cura è con maggiore sicurezza effettuata in ambiente medico di tipo intensivo (medicina d’urgenza o rianimazione).
Altri pazienti presentano sintomatologia neurologica simile-encefalitica con afasia e disturbi del linguaggio. Questi due effetti indesiderati possono essere trattati con corticosteroidi e farmaci anti-interleukina 6 (Tocilizumab).
Sia la CRS che i sintomi neurologici connessi alla terapia CAR-T (ICANS) sono reversibili e scompaiono nella maggioranza dei pazienti nel giro di alcuni giorni.
Le Cellule CAR-T sono una Terapia Viva
Ciò, nel senso che i linfociti CAR-T, una volta infusi nel paziente, sono in grado di sopravvivere e persistere per periodi di tempo prolungati (anche per anni). Questa capacità è particolarmente desiderabile quando il paziente presenta una neoplasia che tende a ripresentarsi a distanza di tempo e quando necessita quindi di ergere uno scudo persistente nel tempo contro focolai minimi residui della malattia.
Le Cellule CAR-T sono una Terapia Prototipo
La terapia CAR-T potrebbe trovare impiego in altre condizioni.
Infatti, i linfociti CD19 positivi hanno un ruolo patogenetico (cioè sono coinvolti nel determinismo della malattia) in molte altre condizioni non maligne.
Nelle malattie autoimmuni severe basate su autoanticorpi, i B linfociti producono autoanticorpi che possono provocare danni all’organismo.
Esempio tipico è una malattia denominata lupus eritematoso sistemico (LES) in cui gli autoanticorpi aggrediscono il rene, il cuore, il polmone, l’encefalo, ciò causa un interessamento sistemico con febbre e citopenie che talvolta non risponde prontamente alla terapia cortisonica o che richiede continua terapia con farmaci immunosoppressori per periodi prolungati.
Un’altra malattia autoimmune sistemica e grave è la sclerosi sistemica, che danneggia molti organi, in primis il polmone e il tubo gastroenterico
In entrambe queste condizioni, frenare i linfociti B con l’impiego di cellule CAR-T anti-CD19 potrebbe essere in grado di incidere positivamente su queste malattie.
| ELARA 2 NHL follicular | phase 2 multinational trial of tisagenlecleucel in adults | R/R FL after ≥2 treatmentrelapsed after an autologous stem cell transplant orafter ≥2 treat. | CR= 69.1% | neurologic events 4.1 % grade ≥3,1% | |
| ZUMA 1NHL linfomarefractory disease | phase 2 trial, we enrolled 111 patients (AXI-CEL) | Diffuse large B-celllymphoma, primary mediastinal B-cell lymphoma, or follicular transformed | CR was 54%Overall response rate 82%, | hypoxia 9%),hypotension (in 9%). | Vasopressors usedin 17%. |
| JULIET istotipo LARGE B CELLDLBC | tisagenlecleucel in a Phase 2 multinational, NCT02445248 | NHL and R/Rrelapsing after autos tx or inelegible to autos. Had received at least two lines of therapy, | 40% of the patients had CR and 12% had PR. | cytokine release syndrome (22%), neurologic events (12%) | |
| ZUMA 5 | AXI-CEL Phase 2 | 148 patients with relapsed/refractory (R/R) indolent (NHL), FL (n=124) and marginal zone lymphoma (MZL) (n=24) | CR=74% | Grade 3 CRS (7%) | grade 3 neurologic (19%). |
La terapia CAR-T potrebbe trovare impiego in futuro anche nel trattamento di altre neoplasie.
Perché ciò si realizzi, bisogna riuscire a individuare un antigene tumorale preferenzialmente espresso sulle cellule neoplastiche e armare i linfociti del paziente con un recettore capace di riconoscere questo antigene.
I linfociti così armati devono essere in grado di penetrare i tessuti neoplastici per svolgere la loro azione. Antigeni preferenzialmente espressi sulle cellule neoplastiche potrebbero essere l’HER-2, il CEA, la mesotelina, la Claudina, il PSA, gli antigeni associati al glioma.
Difficoltà di applicazione nascono, nel caso di neoplasie solide, dal fatto che gli antigeni indicati sono presenti anche in tessuti normali ed è stato osservato che le cellule CAR-T rivolte verso questi antigeni possono danneggiare anche i tessuti sani.
Queste prospettive di nuove applicazioni attendono quindi ulteriori studi volti a perfezionare la terapia rendendola più attiva e più sicura anche in questi ambiti clinici.
Problematiche Logistiche e Aspetti Pratici
Sono rilevanti. Mettere in atto la terapia CAR-T implica il superamento di difficoltà logistiche e di politica sanitaria non indifferenti. È una procedura complessa che prevede passi biologici e clinici che vanno coordinati.
Coinvolge molti attori sia appartenenti a strutture sanitarie sia basati fuori dalle strutture sanitarie. Implica la costruzione di un team in cui medici esperti nella cura di pazienti affetti da mieloma o linfoma si integrino con medici esperti in aferesi e in trapianto emopoietico. Questo team clinico deve poter avere consulenti neurologi addestrati, come pure una pronta disponibilità di posti letto in ambiente medico intensivo.
Le cellule CAR-T dovranno essere, dopo la raccolta aferetica, inviate ad un laboratorio speciale di grado farmacologico per la trasduzione genica necessaria (laboratorio di tipo Cell Factory) e per la successiva moltiplicazione in vitro (espansione cellulare).
Il processo durerà per un mese circa.
Dopo la trasduzione virale del recettore chimerico prescelto, le cellule CAR-T saranno conservate in azoto liquido nella struttura che tratterà il paziente. La degenza e la terapia verranno programmate all’interno di un Programma di Trapianto Emopoietico (come stabilito dalla regolamentazione europea e italiana). Dei dati biologici e clinici dovranno essere strettamente mantenute la tracciabilità e le registrazioni dei controlli qualitativi effettuati.
Un coordinamento che assicuri la gestione complessiva del team è necessario.
Tutto ciò ha anche un costo rilevante, che si aggira su alcune centinaia di miglia di euro a paziente, e che quindi costituisce uno scoglio che fa’ sì che l’accesso alla terapia sia notevolmente ristretto.
Indicazioni Previste (Ottobre 2025)
Linfoma Diffuso a Grandi Cellule (DLBCL)
| Farmaco | Target | Indicazione | Linee precedenti richieste | Risposta globale (ORR) | Risposta completa (CR) | Produttore |
| Axicabtagene ciloleucel (Yescarta®) | CD19 | DLBCL refrattario o recidiva precoce (<12 mesi) dopo 1 o ≥2 linee | ≥1 | 83% | 58% | Kite/Gilead |
| Lisocabtagene maraleucel (Breyanzi®) | CD19 | DLBCL refrattario/recidivante | ≥2 | 73% | 53% | Bristol Myers Squibb |
| Tisagenlecleucel (Kymriah®) | CD19 | DLBCL recidivante o refrattario dopo ≥2 linee | ≥2 | 52% | 40% | Novartis |
Linfoma Primitivo del Mediastino
| Farmaco | Target | Indicazione | Linee precedenti richieste | ORR | CR | Produttore |
| Axicabtagene ciloleucel (Yescarta®) | CD19 | Linfoma primitivo del mediastino refrattario o recidivato | ≥2 | 81% | 54% | Kite/Gilead |
Linfoma Follicolare
| Farmaco | Target | Indicazione | Linee precedenti richieste | ORR | CR | Produttore |
| Axicabtagene ciloleucel (Yescarta®) | CD19 | FL recidivante o refrattario dopo ≥2 linee (incluso anti-CD20 + alchilante) | ≥2 | 94% | 79% | Kite/Gilead |
| Tisagenlecleucel (Kymriah®) | CD19 | FL recidivante o refrattario dopo ≥2 linee | ≥2 | 86% | 69% | Novartis |
Linfoma Mantellare
| Farmaco | Target | Indicazione | Linee precedenti richieste | ORR | CR | Produttore |
| Brexucabtagene autoleucel (Tecartus®) | CD19 | MCL recidivante o refrattario dopo BTKi (ibrutinib/acalabrutinib) e chemioterapia | ≥2 | 93% | 67% | Kite/Gilead |
Linfoma di Hodgkin
| Farmaco | Target | Indicazione (studi in corso) | Stato approvazione | Note |
| Anti-CD30 CAR-T (diversi costrutti) | CD30 | Hodgkin classico refrattario a brentuximab e inibitori PD-1 | In sperimentazione clinica | Risposte CR fino al 70% nei trial di fase I/II |
Indicazioni nel Mieloma Multiplo
| Nome commerciale | Nome internazionale | Target antigenico | Indicazione EMA/FDA | Numero minimo di linee pregresse | Tipo di paziente |
| Abecma® | Idecabtagene vicleucel (ide-cel) | BCMA | RRMM dopo ≥3 linee (IMiD, PI, anti-CD38) | ≥3 | Refrattario o recidivato multiplo |
| Carvykti® | Ciltacabtagene autoleucel (cilta-cel) | BCMA | RRMM dopo ≥1 linea (EMA 2024) | ≥1 | Recidivato dopo lenalidomide o refrattario |
| Arcelis (in sviluppo) | PHE885, CT053, orv-cel | BCMA | Studi clinici fase II-III | — | RRMM |
| Parametro | Requisito |
| Diagnosi | Mieloma multiplo secondo criteri IMWG |
| Pre-trattamento minimo | Fallimento di ≥3 linee terapeutiche (≥1 per cilta-cel secondo EMA 2024) |
| Performance status | ECOG 0-1 (eventualmente 2 se stabilizzato) |
| Funzione ematologica | ANC ≥1.0 ×10⁹/L; PLT ≥50×10⁹/L |
| Funzione renale | eGFR ≥40 mL/min |
| Funzione epatica | AST/ALT ≤3× ULN; bilirubina ≤1.5× ULN |
| Malattia attiva | Evidenza di progressione documentata |
| Infezioni attive | Devono essere escluse o controllate |
| Coinvolgimento SNC | Controindicazione relativa |
| Malattia extramidollare | Ammessa, ma prognosi più sfavorevole |
| Evento avverso | Frequenza | Grado severità | Gestione |
| CRS (Cytokine Release Syndrome) | 70–90% | Grado 1-2 nella maggioranza | Tocilizumab ± desametasone |
| ICANS (neurotossicità) | 10–20% | Grado 1-3 | Corticosteroidi, supporto intensivo |
| Citopenie prolungate | 30–40% | Lieve-moderata | Fattori di crescita, supporto trasfusionale |
| Infezioni opportunistiche | 10–30% | Variabile | Profilassi e sorveglianza |
| Ipogammaglobulinemia | 50% | Cronica | IgEV sostitutive periodiche |
| Studio | CAR-T | N° pazienti | Risposta globale (ORR) | Risposta completa (CR/sCR) | PFS mediana | OS mediana (mesi) |
| KarMMa (NEJM 2021) | Ide-cel | 128 | 73% | 33% | 8.8 | 24.8 |
| CARTITUDE-1 (Lancet 2022) | Cilta-cel | 97 | 98% | 80% | 34.9 | NR (>36 mesi) |
| KarMMa-3 (NEJM 2023) | Ide-cel vs standard | 386 | 71% vs 42% | 33% vs 5% | 13.3 vs 4.4 | 33.5 vs 24.6 |
| CARTITUDE-4 (Lancet 2024) | Cilta-cel (1L recidiva) | 419 | 87% vs 67% | 73% vs 21% | 24.0 vs 11.8 | — |





Lascia un commento